Chlorid meďný
Chlorid meďný (CuCl) je anorganická zlúčenina, jeden z chloridov medi. Ide o bielu tuhú látku zle rozpustnú vo vode, ale dobre rozpustnú v koncentrovanej kyseline chlorovodíkovej. Nečisté vzorky sú zelenkasté vďaka prítomnosti zeleného chloridu meďnatého.[1]
| Chlorid meďný | |||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||
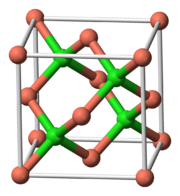 | |||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||
| Sumárny vzorec | CuCl | ||||||||||||||||||||||||||||||||
| Vzhľad | biely prášok | ||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 99,0 u | ||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 98,999 g/mol | ||||||||||||||||||||||||||||||||
| Teplota topenia | 430 °C | ||||||||||||||||||||||||||||||||
| Teplota varu | 1 212 °C | ||||||||||||||||||||||||||||||||
| Hustota | 4,139 g/cm³ | ||||||||||||||||||||||||||||||||
| Rozpustnosť | vo vode: 1,25 g/100 ml v polárnych rozpúšťadlách: kyselina chlorovodíková roztoky amónnych solí roztoky kyanidov | ||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||
| Entropia topenia | 103,5 J/g | ||||||||||||||||||||||||||||||||
| Entropia varu | 219,2 J/g | ||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | −136,5 kJ/mol | ||||||||||||||||||||||||||||||||
| Štandardná entropia | 87,1 J K−1 mol−1 | ||||||||||||||||||||||||||||||||
| Štandardná Gibbsová energia | −114,06 kJ/mol | ||||||||||||||||||||||||||||||||
| Merná tepelná kapacita | 0,489 9 J K−1 g−1 | ||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||
| Číslo CAS | 7758-89-6 | ||||||||||||||||||||||||||||||||
| Číslo UN | 2802 | ||||||||||||||||||||||||||||||||
| EINECS číslo | 231-842-9 | ||||||||||||||||||||||||||||||||
| Číslo RTECS | GL6990000 | ||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||
Vlastnosti upraviť
Chlorid meďný je Lewisova kyselina, klasifikovaná podľa konceptu HSAB ako „mäkká“. Preto má tendenciu tvoriť stabilné komplexy s mäkkými Lewisovými hydroxidmi, napríklad trifenylfosfínom:
- CuCl + P(C6H5)3 → [CuCl(P(C6H5)3)]4
Hoci sa chlorid meďný príliš nerozpúšťa vo vode, rozpúšťa sa vo vodných roztokoch obsahujúcich vhodné donorové molekuly. Tvorí komplexy s halogenidovými iónmi; napríklad s koncentrovanou kyselinou chlorovodíkovou tvorí H3O+CuCl2-. Podobne tvorí komplexy aj s aniónom kyanidu, aniónom tiosíranu a amoniakom.
Roztoky chloridu meďného s chlorovodíkom alebo amoniakom pohlcujú oxid uhoľnatý za vzniku bezfarebných komplexov, napríklad diméru s chloridovým mostíkom [CuCl(CO)]2. Rovnaký roztok s chlorovodíkom reaguje tiež s acetylénom na [CuCl(C2H2)]. Roztok s amoniakom dáva s acetylénom výbušný acetylid meďný. Komplexy chloridu meďného s alkénmi možno pripraviť redukciou chloridu meďnatého oxidom siričitým za prítomnosti alkénu v alkoholovom roztoku. Komplexy s diénmi, napr. 1,5-cyklooktadiénom, sú obzvlášť stabilné:[2]
Za neprítomnosti iných ligandov sú vodné roztoky chlorid meďného nestabilné vzhľadom k disproporcionácii na meď a chlorid meďnatý.[3] Čiastočne z tohto dôvodu sa chlorid meďný na vzduchu sfarbuje dozelena.
Použitie upraviť
Hlavné použitie chloridu meďného je ako prekurzor pre výrobu fungicídneho oxychloridu meďnatého. Na tento účel sa chlorid meďný generuje synproporcionáciu a potom sa oxiduje vzduchom:
- Cu + CuCl2 → 2 CuCl
- 6 CuCl + 3/2 O2 + 3 H2O → 2 Cu3Cl2(OH)4 + CuCl2
Chlorid meďný katalyzuje veľa organických reakcií. Jeho afinita k oxidu uhoľnatému v prítomnosti chloridu hlinitého sa využíva v procese COPureSM.
Organická syntéza upraviť
V Sandmeyerovej reakcii vedie pôsobenie chloridu meďného na aréndiazóniové soli k vzniku arylchloridov, napríklad:[4]
Táto reakcia má široký záber a obvykle ponúka vysokú výťažnosť.
Polyméry upraviť
Chlorid meďný sa používa ako katalyzátor v radikálovej polymerizácii prenosom atómu (ATRP).
Podobné zlúčeniny upraviť
Referencie upraviť
- ↑ United States Patent US4582579 "method of preparing cupric ion free cuprous chloride" Section 2, lines 4-41, via www.freepatentsonline.com
- ↑ Nicholls, D. Complexes and First-Row Transition Elements, Macmillan Press, London, 1973.
- ↑ Greenwood, N.N.; Earnshaw, A. Chemistry of the Elements, 2nd ed., Butterworth-Heinemann, Oxford, UK, 1997.
- ↑ (a) Wade, L. G. Organic Chemistry, 5th ed., p. 871, Prentice Hall, Upper Saddle RIver, New Jersey, 2003. (b) March, J. Advanced Organic Chemistry, 4th ed., p. 723, Wiley, New York, 1992.
Iné projekty upraviť
- Commons ponúka multimediálne súbory na tému Chlorid meďný
Literatúra upraviť
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabuľky. 1. vyd. Praha : Grada Publishing, 1999. ISBN 80-7169-855-5.
- Mellor, J. W., A Comprehensive Treatise on Inorganic and Theoretical Chemistry, Volume III, pp157-168. Longmans, Green & Co., London, 1967 (new impression)
Externé odkazy upraviť
Zdroj upraviť
Tento článok je čiastočný alebo úplný preklad článku Chlorid měďný na českej Wikipédii.




