Lantionín
Lantionín[1] je neproteínogénna aminokyslina. Zvyčajne vzniká z aminokyselín cysteínu a dehydratovaného serínu. Napriek svojmu menu lantionín neobsahuje lantán.
| Lantionín | |
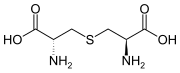 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C6H12N2O4S |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 208,232 g/mol |
| Ďalšie informácie | |
| Číslo CAS | 922-55-4 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
História
upraviťLantionín bol prvýkrát izolovaný v roku 1941 pôsobením uhličitanom sodným na vlnu. Zistilo sa, že je to aminokyselina, ktorá obsahuje síru a preto bola táto aminokyselina pomenovaná lantionín (z latinského lana, vlna, a gréckeho theîon, síra).[2] Lantionín bol prvý raz syntetizovaný alkyláciou cysteínu pomocou β-chlóroalanínu.[3] Lantioníny sú v prírode bežné a boli izolované z ľudských vlasov, laktalbumínu a peria. Lantioníny sa takisto našli v bakteriálnej bunkovej stene a sú súčasťou skupiny peptidových antibiotík zvané lantibiotiká, medzi ktoré patria nizín (konzervant), subtilín, epidermín (účinný proti stafylokokom a streptokokom) a ankovenín (inhibítor enzýmov), ktoré sú geneticky kódované.[4][5]
Syntéza
upraviťBolo publikovaných mnoho spôsobov prípravy lantionínu, napríklad štiepením kruhu serínového β-laktónu,[5] vytlačením síry z cysteínu[6] alebo adíciou cysteínu na dehydroalanín.[7] Metóda vytlačenia síry z cysteínu je však jediná metóda syntézy lantionínu, ktorá bola použitá v celkovej syntéze lantibiotika.
Biosyntézu lantionínového mostíku v prírodných peptidoch je možné dosiahnuť niekoľkými spôsobmi. Napríklad v nizíne sú lantionínové mostíky tvorené dehydratázou (NisB) a cyklázou (NisC).[8][9]
Referencie
upraviť- ↑ BILKOVÁ, Andrea; KIŇOVÁ SEPOVÁ, Hana; BILKA, František. Bakteriocíny produkované baktériami mliečneho kvasenia [online]. proLékaře.cz, [cit. 2022-01-19]. Dostupné online.
- ↑ Horn, M. J.; Jones, D. B.; Ringel, S. J. (1941) Isolation of a New Sulfur-Containing Amino Acid (Lanthionine) from Sodium Carbonate-Treated Wool. Journal of Biological Chemistry, 138, 141-149.
- ↑ Brown, G. B.; du Vigneaud, V. (1941) The Stereoisomeric Forms of Lanthionine. Journal of Biological Chemistry, 140, 767-771.
- ↑ Paul, M.; van der Donk, W. A. (2005) Chemical and Enzymatic Synthesis of Lanthionines. Mini-Reviews in Organic Chemistry, 2, 23-37.
- ↑ a b Shao, H.; Wang, S. H. H.; Lee, C.-W.; Ösapay, G.; Goodman, M. (1995) A Facile Synthesis of Orthogonally Protected Stereoisomeric Lanthionines by Regioselective Ring Opening of Serine β-Lactone Derivatives. Journal of Organic Chemistry, 60, 2956-2957.
- ↑ Harpp, D. N.; Gleason, J. G. (1971) Preparation and Mass Spectral Properties of Cystine and Lanthionine Derivatives. Novel Synthesis of L-Lanthionine by Selective Desulfurization. Journal of Organic Chemistry, 36, 73-80.
- ↑ Probert, J. M.; Rennex, D.; Bradley, M. (1996) Lanthionines for Solid Phase Synthesis. Tetrahedron Letters, 37, 1101-1104.
- ↑ Ribosomally synthesized and post-translationally modified peptide natural products: overview and recommendations for a universal nomenclature. Nat Prod Rep, 2013, s. 108–60. DOI: 10.1039/c2np20085f. PMID 23165928.
- ↑ Discovery, biosynthesis, and engineering of lantipeptides. Annu. Rev. Biochem., 2012, s. 479–505. DOI: 10.1146/annurev-biochem-060110-113521. PMID 22404629.
Pozri aj
upraviťZdroj
upraviťTento článok je čiastočný alebo úplný preklad článku Lanthionine na anglickej Wikipédii.