Alanín
| Tomuto článku alebo sekcii chýbajú odkazy na spoľahlivé zdroje, môže preto obsahovať informácie, ktoré je potrebné ešte overiť. Pomôžte Wikipédii a doplňte do článku citácie, odkazy na spoľahlivé zdroje. |
Alanín (skratka Ala alebo A[1]) je jedna z 20 základných proteínogénnych aminokyselín.[2] Prvýkrát bol izolovaný v roku 1879 z hodvábneho proteínu fibroínu, v ktorom tvorí hlavnú zložku.
| Alanín | |
 | |
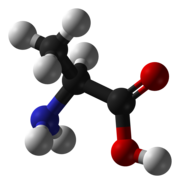 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C3H7NO2 |
| Systematický názov | Kyselina 2-aminopropánová |
| Synonymá | Kyselina α-aminopropiónová, metylglycín |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 89,1 g/mol |
| Teplota varu | 297 °C |
| Hustota | 1,401 g/cm3 |
| pKA | 2,33 9,71 |
| Ďalšie informácie | |
| Číslo CAS | L: 56-41-7 D/L: 302-72-7 D: 338-69-2 |
| SMILES | C[C@@H](C(=O)O)N |
| 3D model (JSmol) | Interaktívny 3D model |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Vlastnosti
upraviťVďaka metylovej skupine je molekula alanínu hydrofóbna. Je druhou najmenšou aminokyselinou po glycíne.[3][4]
Izomér L-alanín otáča rovinu polarizovaného svetla doprava, možno ho teda označiť ako L-(+)-alanín.[2]
Izoméry
upraviťJeho izomér kyselina 3-aminopropánová (β-alanín) sa vo voľnej forme nachádza v ľudskom mozgu a je zložkou niektorých biologicky významných dipeptidov.
Funkcia
upraviťPodieľa sa na metabolizme sacharidov v pečeni a vo svaloch pri fyzickej záťaži. Tvorí spojku medzi laktátom a glukózou, čo je dôležité pri tvorbe glykogénu a v glukózo-alanínovom cykle. Zúčastňuje sa metabolizmu organických kyselín. Je dôležitý pri premene energetických látok v Krebsovom cykle, syntetizuje sa transamináciou z pyruvátu. Spolu s glycínom má pomerne veľké zastúpenie v ľudskej plazme. Stimuluje produkciu imonoglobulínov. Stabilizuje činnosť prostaty.
Syntéza a rozklad
upraviťLaboratórna výroba
upraviťZískava sa hydrolýzou fibroínu, synteticky z acetaldehydu a kyanovodíka (alternatívne z acetanhydridu, acetonitrilu a zo syntézneho plynu) alebo izoláciou z biomasy vznikajúcej bakteriálnym kvasením ropných produktov.
Biosyntéza a rozklad
upraviťAlanín sa v tele premieňa na pyruvát pomocou transaminačnej reakcie.[5] Rovnakým procesom dochádza k jeho rozkladu, a to premenou naspäť na pyruvát.[5]
Okrem toho vzniká alanín i pri rozklade fenylalanínu pôsobením enzýmu kynureninázy.[2]
Použitie
upraviťPoužíva sa v poľnohospodárstve ako súčasť kŕmnych zmesí.
Referencie
upraviť- ↑ Nomenclature and Symbolism for Amino Acids and Peptides [online]. iupac.qmul.ac.uk, [cit. 2023-04-07]. Dostupné online.
- ↑ a b c ŠKÁRKA, Bohumil; FERENČÍK, Miroslav. Biochémia. 3. vyd. [s.l.] : [s.n.], 1992. ISBN 80-05-01076-1. S. 268-306.
- ↑ IMGT Education [online]. www.imgt.org, [cit. 2023-08-26]. Dostupné online.
- ↑ ZAMYATNIN, A A. Amino Acid, Peptide, and Protein Volume in Solution. Annual Review of Biophysics and Bioengineering, 1984-06, roč. 13, čís. 1, s. 145–165. Dostupné online [cit. 2023-08-26]. ISSN 0084-6589. DOI: 10.1146/annurev.bb.13.060184.001045. (po anglicky)
- ↑ a b VOET, Donald. Biochemistry. Hoboken, NJ : John Wiley & Sons, 2011. (4th edition.) Dostupné online. ISBN 978-0-470-57095-1. S. 1030-1068.