Nikotínamidadeníndinukleotid
- Nezamieňať s heslom nikotínamidadeníndinukleotidfosfát.
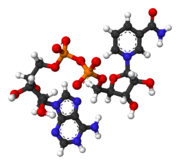
Nikotínamidadeníndinukleotid (NAD) je ústredný kofaktor v metabolizme. Nachádza sa vo všetkých bunkách. NAD je dinukleotid, pretože obsahuje dva nukleotidy spojené fosfátovými skupinami. Jeden nukleotid obsahuje bázu adenín a druhý obsahuje nikotínamid. NAD existuje v dvoch podobách: ako oxidovaná a redukovaná forma, skrátene NAD+ a NADH (H ako vodík). V podobe NAD+ poukazuje „+“ na formálny náboj jedného z dusíkových atómov, ale molekula samotná je v skutočnosti jednomocný anión – s jednotkovým záporným nábojom – pri fyziologickom pH. Naopak NADH je dvojvalentný anión, kvôli dvom mostíkovým fosfátovým skupinám.
| Nikotínamidadeníndinukleotid | |
 | |
 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C21H27N7O14P2 |
| Synonymá | NAD, NAD+, NADH |
| Vzhľad | Biely prášok |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 663,43 g/mol |
| Teplota topenia | 160 °C |
| Ďalšie informácie | |
| Číslo CAS | 53-84-9 53-59-8 (fosfát) 58-68-4 (NADH) |
| PubChem | 925 |
| ChemSpider | 5681 |
| SMILES | O=C(N)c1ccc[n+](c1)[C@@H]2O[C@@H]([C@@H](O)[C@H]2O)COP([O-])(=O)OP(=O)([O-])OC[C@H]5O[C@@H](n4cnc3c(ncnc34)N)[C@H](O)[C@@H]5O |
| 3D model (JSmol) | Interaktívny 3D model |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
V metabolizme je nikotínamidadeníndinukleotid súčasťou redoxných reakcií a prenáša elektróny z jednej reakcie do druhej. Ako kofaktor sa teda v bunkách nachádza v dvoch formách: NAD+ je oxidačné činidlo – prijíma elektróny od iných molekúl, čím sa redukuje. V tejto reakcii sa tvorí NADH, ktorý potom vystupuje ako redukčné činidlo a odovzdáva elektróny. Tieto reakcie, pri ktorých sa presúvajú elektróny, sú hlavnou funkciou NAD. NAD však vystupuje i v iných bunkových procesoch predovšetkým ako substrát enzýmov, ktoré pridávajú alebo odštepujú funkčné skupiny na alebo z bielkovín v posttranslačných úpravách. Kvôli dôležitosti týchto reakcii sú enzýmy vystupujúce v metabolizme NAD cieľom pre nové liečivá.
V organizmoch je možné syntetizovať NAD z jednoduchých základných molekúl (de novo), a to z aminokyselín tryptofánu alebo aspartátu. Alternatívne sú zložitejšie časti koenzýmov prijímané z potravy, napríklad v podobe niacínu. Podobné molekuly sú takisto produkované reakciami, ktoré rozkladajú štruktúru NAD, takže je z nich možné recyklovať a znovu získať aktívnu formu NAD.
NAD sa sčasti konvertuje na koenzým nikotínamidadeníndinukleotidfosfát (NADP). Chemické reakcie NADP sú veľmi podobné NAD, ale NADP vystupuje hlavne ako kofaktor v anabolickom metabolizme.
Fyzikálne a chemické vlastnosti
upraviťNikotínamidadeníndinukleotid pozostáva z dvoch nukleozidov spojených mostíkovými fosfátovými skupinami. Každý nukleozid obsahuje ribózový kruh, jeden s adenínom naviazaným na prvý uhlík (pozíciu 1') cukru (adenozíndifosfátribóza) a druhý s nikotínamidom na danej pozícii. Nikotínamidová skupina môže byť na tento anomérny uhlík pripojená v dvoch rôznych orientáciách. Kvôli týmto dvom možným štruktúram existuje NAD ako dva diastereoméry. V organizmoch sa nachádza β-nikotínamidový diastereomér NAD+. Tieto nukleotidy sú spojené fosfátovými skupinami na uhlíku 5'.[1]
V metabolizme táto zlúčenina prijíma a odovzdáva elektróny v redoxných reakciách.[2] Tieto reakcie spočívajú v odobraní dvoch vodíkových atómov z reaktantu (R) v podobe hydridového aniónu (H-) a protónu (H+). Protón sa rozpustí v roztoku, zatiaľ čo reduktant RH2 sa oxiduje a NAD+ sa redukuje na NADH presunom hydridu na nikotínamidový kruh:
- RH2 + NAD+ → NADH + H+ + R
Z elektrónového páru hydridu je jeden elektrón presunutý na kladne nabitý dusík nikotínamidového kruhu NAD+ a druhý vo vodíkovom atóme je presunutý na C4 uhlík oproti dusíku. Elektrodový potenciál redoxného páru NAD+/NADH je -0,32 V, čo z NADH robí silné redukčné činidlo.[3] Táto reakcia je jednoducho reverzibilná, keď NADH redukuje inú molekulu a znovu sa oxiduje na NAD+. Vďaka tomu môže koenzým opakovane prechádzať medzi formami NAD+ a NADH bez spotrebovania.[1]
Všetky podoby tohto koenzýmu sú biele amorfné prášky, ktoré sú hygroskopické a veľmi dobre rozpustné vo vode.[4] Ako pevné látky sú stabilné, ak sú uchovávané v suchu a v tme. Roztoky NAD+ sú bezfarebné a stabilné asi 1 týždeň pri 4 °C a neutrálnom pH, ale rýchlo sa rozkladajú v kyselinách alebo zásadách. Po rozklade tvoria produkty, ktoré inhibujú enzýmy.[5]
NAD+ i NADH silne absorbujú ultrafialové žiarenie kvôli prítomnosti adenínu. Ako príklad, maximum absorpcie NAD+ je pri vlnovej dĺžke 259 nanometrov (nm) s absorpčným koeficientom 16,900 M−1 cm−1. NADH absorbuje aj pri vyšších vlnových dĺžkach s druhým maximom v UV oblasti pri 339 nm a s absorpčným koeficientom 6,220 M−1 cm−1.[6] Tento rozdiel v absorpčných spektrách medzi oxidovanou a redukovanou formou koenzýmu pri vyšších vlnových dĺžkach umožňuje jednoduché meranie premeny jednej formy na druhú pri stanoveniach enzýmov – meraním množstva absorbovaného UV žiarenia pri 340 nm pomocou spektrofotometra možno stanoviť zmenu koncentrácie NADH v roztoku počas reakcie.[6]
NAD+ a NADH sa líšia aj vo svojej fluorescencii. NADH v roztoku má maximum v emisnom spektre pri 340 nm a polčas fluorescencie 0,4 nanosekundy, zatiaľ čo oxidovaná forma koenzýmu nefluoreskuje.[7] Vlastnosti fluorescenčného signálu sa menia pri naviazaní NADH na bielkoviny, takže tieto zmeny je možné využiť na stanovenie disociačných konštánt, ktoré sú užitočné v enzýmovej kinetike.[7][8] Tieto zmeny vo fluorescencii je možné využiť na stanovenie zmien redoxných stavov v živých bunkách pomocou fluorescenčnej mikroskopie.[9]
Koncentrácia a stav v bunkách
upraviťV pečeni potkanov je celková koncentrácia NAD+ a NADH asi 1 μmol/g hmotnosti (vrátane vody), asi desaťnásobok koncentrácie NADP+ a NADPH v tých istých bunkách.[10] Skutočnú koncentráciu NAD+ v bunkovom cytosóle je zložitejšie zmerať, nedávne odhady v zvieracích bunkách sú približne 0,3 mM[11][12] a približne 1,0 až 2,0 mM v kvasinkách.[13] Až 80 % fluorescencie NADH v mitochodnriách je však vo viazanej podobe, takže jeho koncentrácia v roztoku je omnoho nižšia.[14]
Koncentrácia NAD+ je najvyššia v mitochondriách a tvorí 40 – 70 % celkového bunkového NAD+.[15] NAD+ v cytosóle je presunutý do mitochondrie špecifickým membránovým transportným proteínom, keďže tento koenzým nemôže difundovať skrz membrány.[16] Vnútrobunkový polčas života NAD+ je podľa jednej review odhadovaný na 1-2 hodiny,[17] zatiaľ čo iná review dáva rôzne odhady podľa rôznych kompartmentov (oddelených častí buniek): vnútrobunkový polčas 1-4 hodiny, cytoplazmový 2 hodiny a mitochondriový 4-6 hodín.[18]
Rovnováha medzi oxidovanou a redukovanou formou nikotínamidadeníndinukleotidu sa nazýva pomer NAD+/NADH. Tento pomer je dôležitou súčasťou redoxného stavu bunky, miery poukazujúcej na metabolické aktivity a zdravie buniek.[19] Následky pomeru NAD+/NADH sú komplexné, riadia aktivitu niekoľkých kľúčových enzýmov, zahŕňajúc glyceraldehyd-3-fosfátdehydrogenázu a pyruvátdehydrogenázu. V zdravom cicavčom tkanive je pomer voľného NAD+ a NADH v cytoplazme typicky odhadovaný okolo 700:1, pomer je teda výrazne v prospech oxidačných reakcií.[20][21] Pomer celkového NAD+/NADH je omnoho nižší, s odhadmi u cicavcov okolo 3-10.[22] Naproti tomu pomer NADP+/NADPH je bežne okolo 0,005, takže prevažuje podoba NADPH.[23] Tento rozdiel pomerov je kľúčový pre rôzne metabolické úlohy NADH a NADPH.
Biosyntéza
upraviťNAD+ je syntetizovaný dvomi metabolickými dráhami. Produkuje sa buď v de novo dráhe z aminokyselín alebo recyklačnej dráhe pomocou recyklácie komponent ako je nikotínamid naspäť na NAD+. Aj keď väčšina tkaniva u cicavcov syntetizuje NAD+ pomocou recyklačnej dráhy, de novo syntéza prebieha vo väčšej miere v pečeni z tryptofánu a v obličkách a makrofágock z kyseliny nikotínovej.[24]
Produkcia de novo
upraviťVäčšina organizmov syntetizuje NAD+ z jednoduchých zložiek.[2] Konkrétny súbor reakcií sa medzi organizmami líši, ale spoločným znakom je tvorba kyseliny chinolínovej (QA, z anglického quinolinic acid) z aminokyseliny - buď tryptofánu (Trp) u zvierat a niektorých baktérií, alebo aspartátu (Asp) u niektorých baktérií a rastlín.[25][26] Kyselina chinolínová sa mení na mononukleotid kyseliny nikotínovej (NaMN, z anglického nicotinic acid mononucleotide) pomocou transferu fosforibózového zvyšku. Následne je naňho pripojený adenylát za tvorby kyselina nikotínová adeníndinukleotidu (NaAD). Nakoniec sa kyseliny nikotínová amiduje na nikotínamid, čím vzniká nikotínamidadeníndinukleotid (NAD).[2]
V ďalšom kroku sa časť NAD+ konvertuje na NADP+ pomocou enzýmu NAD+ kináza, ktorý fosforyluje NAD+.[27] U väčšiny organizmov tento enzým využíva ATP ako zdroj fosfátu, ale niektoré baktérie, ako napríklad Mycobacterium tuberculosis a hypertermofilný archeón Pyrococcus horikoshii, využívajú polyfosfát ako alternatívny zdroj fosfátu.[28][29]
Obnovovacie dráhy
upraviťNapriek prítomnosti dráhy na syntézu de novo existujú recyklačné reakcie, ktoré sú u človeka dôležité. Nedostatok niacínu v potrave spôsobuje vitamínovú deficienciu (nedostatok) zvanú pelagra.[30] Tento vysoký nárok na NAD+ vychádza z konštantnej spotreby koenzýmu v reakciách ako sú posttranslačne úpravy, keďže cyklovanie NAD+ medzi oxidovanou a redukovanou formou v redoxných reakciách nemení celkové množstvo koenzýmu.[2] Hlavným zdrojom NAD+ u cicavcov sú obnovovacie dráhy, ktoré recykluju nikotínamid produkovaný enzýmami využívajúcimi NAD+.[31] V prvom kroku tejto dráhy, ktorý je zároveň rýchlosť určujúcim krokom, vystupuje enzým nikotínamidfosforibozyltransferáza (NAMPT), ktorá produkuje nikotínamidmononukleotid (NMN).[31] NMN je priamym prekurzorom NAD+ v tejto dráhe.[32]
Okrem skladania NAD+ de novo z jednoduchých aminokyselinových prekurzorov využívajú bunky aj zlúčeniny obsahujúce pyridínový základ. Tri vitamínové prekurzory využívané v recyklačných metabolických dráhach sú kyselina nikotínová (NA), nikotínamid (Nam) a nikotínamidribozid (NR).[2] Tieto zlúčeniny je možné prijať priamo z potreby a sú označované ako vitamín B3 alebo niacín. Tieto zlúčeniny sú však produkované aj priamo v bunke a spotrebou bunkového NAD+. Niektoré enzýmy vystupujúce v týchto obnovovacích dráhach sa zrejme združujú u bunkového jadra, čo môže kompenzovať vysokú spotrebu NAD+ v tejto organele.[33] Podľa niektorých poznatkov môžu bunky cicavcov prijímať extracelulárny NAD+ zo svojho okolia[34] a rovnako môžu byť nikotínamid a nikotínamidribozid prijímané v črevách.[35]
Obnovovacie reakcie prebiehajúce u mikroorganizmov sa líšia od cicavčích.[36] Niektoré patogény, ako kvasinky Candida glabrata a baktéria Haemophilus influenzae, sú NAD+ auxotrofy - nevedia syntetizovať NAD+ - ale majú recyklačné dráhy a teda sú závislé na zdrojoch NAD+ alebo jeho prekurzoroch zo svojho okolia.[37][38] Ešte prekvapujúcejší je vnútrobunkový patogén Chlamydia trachomatis, ktorému chýbajú rozpoznateľní kandidáti na akékoľvek gény vystupujúce v biosyntéze či obnove NAD+ i NADP+, takže musí tieto koenzýmy získavať od svojho hostiteľa.[39]
Funkcie
upraviťNikotínamidadeníndinukleotid má niekoľko dôležitých úloh v metabolizme. Funguje ako koenzým v redoxných reakciích, ako donor ADP-ribózy v ADP-ribozylačných reakciách, ako prekurzor druhého posla cyklickej ADP-ribózy, zároveň vystupuje ako substrát pre bakteriálne DNA ligázy a skupinu enzýmov zvaných sirtuíny, ktoré využívajú NAD+ na odstránenie acetylových skupín z bielkovín. Okrem týchto metabolických funkcií vystupuje NAD+ ako adenínový nukleotid, ktorý môže opustiť bunku spontánnymi a regulovanými mechanizmami,[41][42] takže môže mať dôležité mimobunkové úlohy.[42]
Oxidoreduktázová väzba NAD
upraviťHlavná úloha NAD+ v metabolizme je presun elektrónov z jednej molekuly na druhú. Reakcie tohto typu sú katalyzované veľkou skupinou enzýmov zvaných oxidoreduktázy. Správne názvy týchto enzýmov obsahujú názov oboch ich substrátov: napríklad NADH-ubichinón oxidoreduktáza katalyuje oxidáciu NADH koenzýmom Q.[43] Tieto enzýmy sú však často označované ako dehydrogenázy a reduktázy, napríklad NADH-ubichinón oxidoreduktáza sa bežne nazýva NADH dehydrogenáza alebo koenzým Q reduktáza.[44]
Mnoho rôznych superrodín enzýmov viaže NAD+/NADH. Jedna z najbežnejších superrodín obsahuje štruktúrny motív známy ako Rossmannov fold.[45][46] Tento motív je pomenovaný po Michaelovi Rossmannovi, ktorý si ako prvý vedec všimol ako často sa táto štruktúra nachádza v bielkovinách, ktoré viažu nukleotidy.[47] Príklad bakteriálneho enzýmu vystupujúceho v metabolizme aminokyselín, ktorý viaže NAD a nemá Rossmannov fold, je možné nájsť u Pseudomonas syringae pv. tomato (PDB: 2CWH, InterPro: IPR003767).[48]
Keď sa nikotínamidadeníndinukleotid viaže na aktívne miesto oxidoreduktáz, nikotinamidový kruh koenzýmu je natočený tak, aby mohol prijať hydridový vodík od druhého substrátu. Hydridový donor môže byť u rôznych enzýmov umiestnený „nad“ alebo „pod“ rovinou planárneho C4 uhlíku, ukázaného na obrázku. Oxidoreduktázy triedy A presúvajú hydridový vodík zhora, oxidoreduktázy triedy B ho presúvajú zospodu. Keďže tento C4 uhlík je prochirálny, možno toho využiť u enzýmovej kinetiky a tým zistiť, akým mechanizmom reakcia prebieha. Pri tomto procese sa zmieša enzým so substrátom, ktorý má vodíky substituované za deutérium, takže enzým redukuje NAD+ presunom deutéria namiesto vodíku. Takto môže enzým vytvoriť jeden z dvoch stereomérov NADH.[49] Podľa toho, ktorý stereomér vzniká, sú enzýmy riadené na dve triedy: trieda A (donor je nad rovinou) a trieda B (donor je pod rovinou).
Enzýmy takmer vždy vykazujú vysoký level špecificity buď pre NAD+, alebo NADP+, napriek podobnosti ich väzby na proteín.[50] Táto špecificita sa odráža na rôznych metabolických úlohách týchto koenzýmov a je výsledkom rôznych skupín aminokyselinových reziduí v dvoch druhoch vreciek viažucich koenzýmy. V aktívnom mieste NADP-dependentných enzýmov vzniká iónová väzba medzi bazickým aminokyselinovým postranným reťazcom a kyslou fosfátovou skupinou NADP+. Naopak u NAD-dependentných enzýmov je náboj vo vrecku opačný, čo zabraňuje väzbe NADP+. Exisuje však niekoľko výnimiek, ako sú enzýmy aldózareduktáza, glukóza-6-fosfátdehydrogenáza a metyléntetrahydrofolátreduktáza, ktoré môžu u niektorých druhov využiť oba koenzýmy.[51]
Úloha v redoxnom metabolizme
upraviťRedoxné reakcie katalyzované oxidoreduktázami sú životne dôležité pre všetky časti metabolzmu, ale obzvlášť dôležitou funkciou týchto reakcií je umožniť živinám získať energiu uloženú v relatívne slabej dvojitej väzbe v molekule kyslíku.[52] Redukované zlúčeniny, ako sú glukóza a mastné kyseliny, sú oxidované, čím sa uvoľňuje chemická energia z O2. Pri tomto procese sa NAD+ redukuje na NADH v procesoch glykolýzy, beta-oxidácie a citrátového cyklu. U eukaryotov sú elektróny prenášané na NADH, ktorý sa tvorí v cytoplazme a následne sa presúva do mitochondrie (na redukciu mitochondriálneho NAD+) pomocou mitochondriálnych člnkov, ako je glycerolfosfátový člnok[53] alebo malát-aspartátový člnok.[54] Mitochondriálny NADH je potom oxidovaný v dýchacom reťazci, ktorý prenáša protóny cez membránu a vytvára ATP pomocou oxidačnej fosforylácie.[55] Tieto člnkové systémy majú rovnakú transportnú funkciu aj v chloroplastoch.[56]
Keďže oxidovaná i redukovaná forma nikotínamidadeníndinukleotidu je využívaná u týcho spojených skupín reakcií, bunka udržiava vysokú koncentráciu NAD+ i NADH. Vysoký pomer NAD+/NADH umožňuje tomuto koenzýmu vystupovať ako oxidačné i redukčné činidlo.[57] Naproti tomu NADPH vystupuje hlavne ako redukčné činidlo v anabolizme, a to v dráhach ako je syntéza mastných kyselín alebo fotosyntéza. Keďže NADPH je nutné ako silné redukčné činidlo, aby mohli prebiehať redoxné reakcie, je udržiavaný veľmi nízky pomer NADP+/NADPH.[57]
Aj keď je NADH dôležité v katabolizme, objavuje sa i v anabolických reakciách, ako napríklad glukoneogenéze.[58] Potreba NADH v anabolizme vytvára problém pre prokaryoty rastúce zo živín, ktoré poskytujú len malé množstvo energie. Nitrifikačné baktérie, ako napríklad rod Nitrobacter, oxidujú dusitany na dusičnany, čím sa uvoľňuje dostatočné množstvo energie na presun protónov a tvorbu ATP, ale nie na priamu produkciu NADH.[59] Keďže NADH je i tak vyžadované u anabolických reakcií, tieto baktére využívajú nitritoxidoreduktázu na tvorbu dostatočnej protónmotívnej sily (protónového gradientu), aby mohla časť dýchacieho reťazca bežať v opačnom smere a mohlo sa tvoriť NADH.[60]
Neredoxné reakcie
upraviťKoenzým NAD+ je takisto spotrebovaný v reakciách, kde dochádza k presunu ADP-ribózy. Enzýmy zvané ADP-ribozyltransferázy presúvajú ADP-ribózovú skupinu z tejto molekuly na bielkoviny v posttranslačnej úprave nazývanej ADP-ribozylácia.[61] ADP-ribozylácia pozostáva buď z presunu jednej ADP-ribózovej jednotky, teda sa jedná o mono-ADP-ribozyláciu, alebo presunu ADP-ribózy na bielkoviny v podobe dlhých vetvených reťazcov, čo sa nazýva poly(ADP-ribozyl)ácia.[62] Mono-ADP-ribozylácia bola prvýkrát identifikovaná ako mechanizmus pôsobenia skupiny bakteriálnych toxínov, hlavne toxínu cholery, ale prebieha i u bežnej bunkovej signalizácie.[63][64] Poly(ADP-ribozyl)áciu vykonávajú poly(ADP-ribóza)polymerázy.[62][65] Štruktúra poly(ADP-ribózy) je využívaná v regulácii niekoľkých bunkových dejov a je najdôležitejšia v bunkovom jadre, v procesoch ako sú oprava DNA a údržba telomér.[65] Okrem týchto funkcií v bunke bola nedávno objavená skupina extracelulárnych ADP-ribozyltransferáz, ale ich úloha ostáva nejasná.[66] NAD+ môže byť pridané i na bunkovú RNA ako 5'-terminálna modifikácia.[67]
Ďalšia funkcia tohto koenzýmu v bunkovej signalizácii je, že slúži ako prekurzor cyklickej ADP-ribózy, ktorá sa produkuje z NAD+ pomocou ADP-ribozylcykláz ako šúčasť systému druhých poslov.[68] Táto molekula pôsobí vo vápnikovej signalizácii uvoľnením vápniku z intracelulárnych zásob.[69] Viaže sa na takzvané ryanodínové receptory, umiestnené na membránach organel, ako je napríklad endoplazmatické retikulum, čím dochádza k otvoreniu týchto vápnikových kanálov.[70]
NAD+ spotrebovávajú i sirtuíny, čo sú NAD-dependentné deacetylázy, ako je Sir2.[71] Tieto enzýmy presúvajú acetylovú skupinu zo substrátového proteínu na ADP-ribózovú zložku NAD+, čo rozštiepi tento koenzým a uvoľní nikotínamid a O-acetyl-ADP-ribózu. Sirtuíny zjavne vystupujú hlavne v regulácii transkripcie pomocou deacetylácie histónov a zmeny štruktúry nukleozómu.[72] Sirtuíny však môžu deacetylovať i nehistónové bielkoviny. Táto aktivita sirtuínov je zaujímavá predovšetkým kvôli jej dôležitosti v regulácii procesu starnutia.[73]
Ďalšie NAD-dependentné enzýmy zahŕňajú bakteriálne DNA ligázy, ktoré spájajú dva konce DNA s využitím NAD+ ako substrátu, ktorý dodáva adenozínmonofosfát (AMP) na 5' fosfátovú skupinu jedného konca DNA. Na tento intermediát sa potom viaže 3' hydroxylová skupina druhého konca DNA, čím vzniká fosfodiesterová väzba.[74] Naproti tomu eukaryotické DNA ligázy využívajú ATP na tvorbu DNA-AMP intermediátu.[75]
Li et al. zistili, že NAD+ priamo reguluje proteín-proteínové interakcie.[76] Takisto ukázali, že jeden z dôvodov poklesu opráv DNA spojených so starobou by mohla byť zvýšená väzba proteínu DBC1 (Deleted in Breast Cancer 1, „vymazaný pri rakovine prsníka 1“) na PARP1 (poly(ADP-ribóza)polymeráza 1), keďže pri starnutí sa znižuje hladina NAD+.[76] Úprava hladiny NAD+ by teda mohla ochrániť pred rakovinou, radiáciou a starnutím.[76]
Extracelulárne pôsobenie NAD+
upraviťV posledných rokoch bol NAD+ odhalený ako extracelulárna signalizačná molekula, ktorá vystupuje v medzibunkovej komunikácii.[42][77][78] NAD+ sa uvoľňuje z neurónov v cievach,[41] močovom mechúre,[41][79] hrubom čreve,[80][81] z neurosekrečných buniek[82] a mozgových synaptozómov[83] a bol navrhnutý ako nový neurotransmiter, ktorý prenáša informáciu z nervov na efektorové bunky v orgánoch s hladkou svalovinou.[80][81] U rastlín indukuje extracelulárny nikotínamidadeníndinukleotid rezistenciu voči patogénnej infekcii a bol identifikovaný prvý extracelulárny receptor NAD.[84] Ďalšie výskumy sú nutné na určenie základných mechanizmov jeho extracelulárneho pôsobenia a ich dôležitosti pre zdravie človeka a životné procesy u ostatných organizmov.
Klinický význam
upraviťEnzýmy, ktoré tvoria a využívajú NAD+ a NADH, sú dôležité pre farmakológiu i pre výskum novej liečby chorôb.[85] Dizajn liekov a vývoj liekov využíva NAD+ tromi spôsobmi: ako priamy cieľ pôsobenia liekov, dizajnovaním enzýmových inhibítorov alebo aktivátorov založených na jeho štruktúre, ktoré menia aktivitu NAD-dependentných enzýmov, a snahou inhibovať biosyntézu NAD+.[86]
Keďže rakovinové bunky využívajú glykolýzu v zvýšenej miere a keďže NAD podporuje glykolýzu, nikotínamidfosforibozyltransferáza (obnovovacia dráha NAD) je často zvýšená v rakovinových bunkách.[87][88]
NAD bol študovaný pre potenciálne použitie v terapii neurodegeneratívnych porúch, ako je napríklad Alzheimerova alebo Parkinsonova choroba.[2] Klinické skúšky (bez prekurzorov NAD) s kontrolnou skupinou s placebom, ktoré testovali efekt NADH, nepreukázali žiadny efekt u ľudí s Parkinsonovou chorobou.[89]
NAD+ je takisto cieľom liekčiva izoniazid, ktorý sa používa pri liečbe tuberkulózy, infekcie spôsobenej baktériou Mycobacterium tuberculosis. Izoniazid je „prodrug“ (liek, ktorého aktívna forma vzniká ako metabolit v tele) a keď sa dostane do baktérie, je aktivovaný peroxidázovým enzýmom, ktorý túto zlúčeninu oxiduje do podoby voľného radikálu.[90] Tento radikál potom reaguje s NADH, čím vznikajú adukty, ktoré pôsobia ako veľmi silné inhibítory enzýmu enoyl-acyl carrier protein reduktázy[91] a dihydrofolátreduktázy.[92]
Keďže mnoho oxidoreduktáz využíva NAD+ a NADH ako substráty a viažu ich pomocou vysoko konzervovaných štruktúrnych motívov, je prekvapivá predstava, že by inhibítory založené na NAD+ mohli byť špecifické pre konkrétny enzým.[93] Napriek tomu je to však možné - napríklad inhibítory založené na zlúčeninách ako kyselina mykofenolová a tiazofurín inhibujú IMP dehydrogenázu na väzbovom mieste pre NAD+. Tento enzým je dôležity v metabolizme purínov, takže sa tieto molekuly dajú využiť ako lieky proti rakovine, vírusom, alebo ako imunosupresíva.[93][94] Iné lieky nie sú enzýmové inhibítory, ale namiesto toho aktivujú enzýmy vystupujúce v metabolizme NAD+. Sirtuíny sú obzvlášť zaujímavým cieľom týchto liekov, keďže aktivácia týchto NAD-dependentných acetyláz v niektorých zvieracích modeloch predlžuje život.[95] Zlúčeniny ako resveratrol zvyšujú aktivitu týchto enzýmov, čo môže hrať dôležitú úlohu v ich schopnosti oddialiť starnutie v modelových organizmoch ako u stavovcoch,[96][97] tak i u bezstavovcov.[98] V jednom experimente sa u myší, ktorým bol podávaný NAD po dobu jedného týždňa, zlepšila komunikácia medzi jadrom a mitochondriami.[99]
Vďaka rozdielom v metabolických dráhach biosyntézy NAD+ u rôznych organizmov, napríklad baktérií a človeka, je táto oblasť metabolizmu veľmi sľubnou oblasťou pre vývoj nových antibiotík.[100][101] Napríklad enzým nikotínamidáza, ktorá premieňa nikotínamid na kyselinu nikotínovú, je cieľom pre dizajn liečiv, keďže tento enzým sa nachádza u kvasiniek a baktérií, ale nie je prítomný u človeka.[36]
V bakteriológii sa občas NAD označuje ako faktor V a využíva sa ako doplnok pre kultivačné média pre niektoré baktérie so špecifickými rastovými nárokmi.[102]
História
upraviťKoenzým NAD+ prví objavili birtskí biochemici Arthur Harden a William John Young v roku 1906.[103] Všimli si, že prídavok povareného a filtrovaného extraktu kvasiniek zrýchlil priebeh alkoholového kvasenia v nepovarenom extraktu kvasiniek. Neidentifikovaný faktor zodpovedný za tento efekt pomenovali koferment. Po dlhej a náročnej purifikácii extraktu kvasiniek bol tento teplu odolný faktor identifikovaný Hansom von Euler-Chelpinom ako nukleotid-cukor-fosfát.[104] V roku 1936 ukázal nemecký vedec Otto Heinrich Warburg úlohu tohto nukleotidového koenzýmu v prenose hydridu a identifikoval nikotínamidovú zložku ako miesto priebehu redoxných reakcií.[105]
Vitamínové prekurzory NAD+ boli prvýkrát identifikované v roku 1938, keď Conrad Elvehjem ukázal, že pečeň má účinok „proti čiernemu jazyku“ („anti-black tongue“) v podobe nikotínamidu.[106] Následne v roku 1939 predniesol prvý dôkaz, že niacín sa využíva pri syntéze NAD+.[107] Začiatkom 40. rokov 20. storočia bol Arthur Kornberg prvý, kto detegoval enzým v biosyntetickej dráhe.[108] V roku 1949 potom americkí biochemici Morris Friedkin a Albert L. Lehninger dokázali, že NADH prepája metabolické dráhy ako sú citrátový cyklus so syntézou ATP v oxidačnej fosforylácii.[109] V roku 1958 objavili Jack Preiss and Philip Handler intermediáty a enzýmy vystupujúce v biosyntéze NAD+[110][111] - obnovovacia dráha z kyseliny nikotínovej sa označuje ako Preiss-Handlerova dráha.V roku 2004 odhalili Charles Brenner a jeho spolupracovníci nikotínamidribozidkinázovú dráhu syntézy NAD+.[112]
Neredoxné úlohy NAD(P) boli objavené neskôr.[1] Ako prvá bola identifikovaná úloha NAD+ ako ADP-ribózového donoru v ADP-ribozylačných reakciách pozorovaných na začiatku 60. rokov 20. storočia.[113] Štúdie v priebehu 80. a 90. rokov odhalili aktivitu metabolitov NAD+ a NADP+ v bunkovej signalizácii - ako je aktivita cyklickej ADP-ribózy, ktorá bola objavená v roku 1987.[114]
Metabolizmus NAD+ ostal oblasťou intenzívneho výskumu i v 21. storočí a záujem sa ešte zvýšil po objave NAD-dependentných proteínových deacetyláz nazývaných sirtuíny v roku 2000, ktoré objavil Shin-ichiro Imai a jeho spolupracovníci v laboratóriu Leonarda P. Guarenteho.[115] V roku 2009 Imai predložil „NAD Svet“ („NAD World“) hypotézu, podľa ktorej sú kľúčovými regulátormi starnutia a dlhovekosti cicavcov sirtuín 1 a primárny enzým syntézy NAD+, nikotínamidfosforibozyltransferáza (NAMPT).[116] V roku 2016 potom Imai hypotézu rozšíril na „NAD Svet 2.0“, ktorý postuluje to, že extracelulárna NAMPT z adipózneho tkaniva udržiava NAD+ v hypotalame (kontrolnom centre) v spojení s myokínmi z buniek kostrových svalov.[117]
Referencie
upraviť- ↑ a b c The power to reduce: pyridine nucleotides – small molecules with a multitude of functions. Biochem. J., 2007, s. 205–18. DOI: 10.1042/BJ20061638. PMID 17295611.
- ↑ a b c d e f NAD+ metabolism in health and disease. Trends Biochem. Sci., 2007, s. 12–9. Dostupné online [cit. 2007-12-23]. DOI: 10.1016/j.tibs.2006.11.006. PMID 17161604.
- ↑ Alternative respiratory pathways of Escherichia coli: energetics and transcriptional regulation in response to electron acceptors. Biochim. Biophys. Acta, 1997, s. 217–34. DOI: 10.1016/S0005-2728(97)00034-0. PMID 9230919.
- ↑ Windholz, Martha. The Merck Index: an encyclopedia of chemicals, drugs, and biologicals. 10th. vyd. Rahway NJ, US : Merck, 1983. ISBN 978-0-911910-27-8. S. 909.
- ↑ Structure of lactate dehydrogenase inhibitor generated from coenzyme. Biochemistry, 1979, s. 1212–7. DOI: 10.1021/bi00574a015. PMID 218616.
- ↑ a b Dawson, R. Ben. Data for biochemical research. 3rd. vyd. Oxford : Clarendon Press, 1985. ISBN 978-0-19-855358-8. S. 122.
- ↑ a b Fluorescence lifetime imaging of free and protein-bound NADH. Proc. Natl. Acad. Sci. U.S.A., 1992, s. 1271–5. DOI: 10.1073/pnas.89.4.1271. PMID 1741380.
- ↑ Time-resolved fluorescence studies on NADH bound to mitochondrial malate dehydrogenase. Biochim. Biophys. Acta, 1989, s. 187–90. DOI: 10.1016/0167-4838(89)90159-3. PMID 2910350.
- ↑ The Free NADH Concentration Is Kept Constant in Plant Mitochondria under Different Metabolic Conditions. Plant Cell, 2006, s. 688–98. DOI: 10.1105/tpc.105.039354. PMID 16461578.
- ↑ Measurement of tissue purine, pyrimidine, and other nucleotides by radial compression high-performance liquid chromatography. Anal. Biochem., 1984, s. 162–71. DOI: 10.1016/0003-2697(84)90148-9. PMID 6486402.
- ↑ The simultaneous measurement of nicotinamide adenine dinucleotide and related compounds by liquid chromatography/electrospray ionization tandem mass spectrometry. Anal. Biochem., 2006, s. 282–5. DOI: 10.1016/j.ab.2006.02.017. PMID 16574057.
- ↑ Nutrient-Sensitive Mitochondrial NAD+ Levels Dictate Cell Survival. Cell, 2007, s. 1095–107. DOI: 10.1016/j.cell.2007.07.035. PMID 17889652.
- ↑ Nicotinamide riboside promotes Sir2 silencing and extends lifespan via Nrk and Urh1/Pnp1/Meu1 pathways to NAD+. Cell, 2007, s. 473–84. DOI: 10.1016/j.cell.2007.03.024. PMID 17482543.
- ↑ Distribution of mitochondrial NADH fluorescence lifetimes: steady-state kinetics of matrix NADH interactions. Biochemistry, 2005, s. 2585–94. DOI: 10.1021/bi0485124. PMID 15709771.
- ↑ Regulation of Glucose Metabolism by NAD + and ADP-Ribosylation. Cells, 2019, s. 890. DOI: 10.3390/cells8080890. PMID 31412683.
- ↑ Identification of the mitochondrial NAD+ transporter in Saccharomyces cerevisiae. J. Biol. Chem., 2006, s. 1524–31. DOI: 10.1074/jbc.M510425200. PMID 16291748.
- ↑ Srivastava S. Emerging therapeutic roles for NAD(+) metabolism in mitochondrial and age-related disorders. Clinical and Translational Medicine, 2016, s. 25. DOI: 10.1186/s40169-016-0104-7. PMID 27465020.
- ↑ Regulatory Effects of NAD + Metabolic Pathways on Sirtuin Activity. Progress in Molecular Biology and Translational Science, 2018, s. 71–104. DOI: 10.1016/bs.pmbts.2017.11.012. PMID 29413178.
- ↑ Redox environment of the cell as viewed through the redox state of the glutathione disulfide/glutathione couple. Free Radic Biol Med, 2001, s. 1191–212. DOI: 10.1016/S0891-5849(01)00480-4. PMID 11368918.
- ↑ The redox state of free nicotinamide-adenine dinucleotide in the cytoplasm and mitochondria of rat liver. Biochem. J., 1967, s. 514–27. DOI: 10.1042/bj1030514. PMID 4291787.
- ↑ Regulation of corepressor function by nuclear NADH. Science, 2002, s. 1895–7. DOI: 10.1126/science.1069300. PMID 11847309.
- ↑ Nicotinamide adenine dinucleotide, a metabolic regulator of transcription, longevity and disease. Curr. Opin. Cell Biol., April 2003, s. 241–6. DOI: 10.1016/S0955-0674(03)00006-1. PMID 12648681.
- ↑ The redox state of free nicotinamide–adenine dinucleotide phosphate in the cytoplasm of rat liver. Biochem. J., 1969, s. 609–19. DOI: 10.1042/bj1150609a. PMID 4391039.
- ↑ Age-related NAD + decline. Experimental Gerontology, 2020, s. 110888. DOI: 10.1016/j.exger.2020.110888. PMID 32097708.
- ↑ Early Steps in the Biosynthesis of NAD in Arabidopsis Start with Aspartate and Occur in the Plastid. Plant Physiol., 2006, s. 851–7. DOI: 10.1104/pp.106.081091. PMID 16698895.
- ↑ Nicotinamide adenine dinucleotide biosynthesis and pyridine nucleotide cycle metabolism in microbial systems. Microbiol. Rev., 1 March 1980, s. 83–105. DOI: 10.1128/MMBR.44.1.83-105.1980. PMID 6997723.
- ↑ Structural and functional properties of NAD kinase, a key enzyme in NADP biosynthesis. Mini Reviews in Medicinal Chemistry, 2006, s. 739–46. DOI: 10.2174/138955706777698688. PMID 16842123.
- ↑ First Archaeal Inorganic Polyphosphate/ATP-Dependent NAD Kinase, from Hyperthermophilic Archaeon Pyrococcus horikoshii: Cloning, Expression, and Characterization. Appl. Environ. Microbiol., 2005, s. 4352–8. DOI: 10.1128/AEM.71.8.4352-4358.2005. PMID 16085824.
- ↑ Characterization of Mycobacterium tuberculosis NAD kinase: functional analysis of the full-length enzyme by site-directed mutagenesis. Biochemistry, 2004, s. 7610–7. DOI: 10.1021/bi049650w. PMID 15182203.
- ↑ Henderson LM. Niacin. Annu. Rev. Nutr., 1983, s. 289–307. DOI: 10.1146/annurev.nu.03.070183.001445. PMID 6357238.
- ↑ a b Therapeutic Potential of NAD-Boosting Molecules: The In Vivo Evidence. Cell Metabolism, 2018, s. 529–547. DOI: 10.1016/j.cmet.2018.02.011. PMID 29514064.
- ↑ What is NMN? [online]. . Dostupné online.
- ↑ Manipulation of a nuclear NAD+ salvage pathway delays aging without altering steady-state NAD+ levels. J. Biol. Chem., 2002, s. 18881–90. DOI: 10.1074/jbc.M111773200. PMID 11884393.
- ↑ Characterization of NAD Uptake in Mammalian Cells. J. Biol. Chem., 2008, s. 6367–74. DOI: 10.1074/jbc.M706204200. PMID 18180302.
- ↑ Nicotinamide riboside is uniquely and orally bioavailable in mice and humans. Nature Communications, 2016, s. 12948. DOI: 10.1038/ncomms12948. PMID 27721479.
- ↑ a b Reconstructing eukaryotic NAD metabolism. BioEssays, 2003, s. 683–90. DOI: 10.1002/bies.10297. PMID 12815723.
- ↑ Assimilation of NAD+ precursors in Candida glabrata. Mol. Microbiol., 2007, s. 14–25. DOI: 10.1111/j.1365-2958.2007.05886.x. PMID 17725566.
- ↑ NADP and NAD utilization in Haemophilus influenzae. Mol. Microbiol., 2000, s. 1573–81. DOI: 10.1046/j.1365-2958.2000.01829.x. PMID 10760156.
- ↑ From Genetic Footprinting to Antimicrobial Drug Targets: Examples in Cofactor Biosynthetic Pathways. J. Bacteriol., 2002, s. 4555–72. DOI: 10.1128/JB.184.16.4555-4572.2002. PMID 12142426.
- ↑ Crystallization of three key glycolytic enzymes of the opportunistic pathogen Cryptosporidium parvum. Biochim. Biophys. Acta, 2005, s. 166–72. DOI: 10.1016/j.bbapap.2005.04.009. PMID 15953771.
- ↑ a b c Release of beta-nicotinamide adenine dinucleotide upon stimulation of postganglionic nerve terminals in blood vessels and urinary bladder. J Biol Chem, 2004, s. 48893–903. DOI: 10.1074/jbc.M407266200. PMID 15364945.
- ↑ a b c Emerging functions of extracellular pyridine nucleotides. Mol. Med., 2006, s. 324–7. DOI: 10.2119/2006-00075.Billington. PMID 17380199.
- ↑ Enzyme Nomenclature, Recommendations for enzyme names from the Nomenclature Committee of the International Union of Biochemistry and Molecular Biology [online]. . Dostupné online. Archivované 2007-12-05 z originálu.
- ↑ NiceZyme View of ENZYME: EC 1.6.5.3 [online]. Expasy. Dostupné online.
- ↑ Proteopedia: Rossmann fold: A beta-alpha-beta fold at dinucleotide binding sites. Biochem Mol Biol Educ, 2015, s. 206–209. DOI: 10.1002/bmb.20849. PMID 25704928.
- ↑ Lesk AM. NAD-binding domains of dehydrogenases. Curr. Opin. Struct. Biol., 1995, s. 775–83. DOI: 10.1016/0959-440X(95)80010-7. PMID 8749365.
- ↑ Comparison of super-secondary structures in proteins. J Mol Biol, 1973, s. 241–56. DOI: 10.1016/0022-2836(73)90388-4. PMID 4737475.
- ↑ Crystal structures of Delta1-piperideine-2-carboxylate/Delta1-pyrroline-2-carboxylate reductase belonging to a new family of NAD(P)H-dependent oxidoreductases: conformational change, substrate recognition, and stereochemistry of the reaction. J. Biol. Chem., 2005, s. 40875–84. DOI: 10.1074/jbc.M507399200. PMID 16192274.
- ↑ a b Bellamacina CR. The nicotinamide dinucleotide binding motif: a comparison of nucleotide binding proteins. FASEB J., 1 September 1996, s. 1257–69. DOI: 10.1096/fasebj.10.11.8836039. PMID 8836039.
- ↑ NADP-dependent enzymes. I: Conserved stereochemistry of cofactor binding. Proteins, 1997, s. 10–28. DOI: 10.1002/(SICI)1097-0134(199705)28:1<10::AID-PROT2>3.0.CO;2-N. PMID 9144787.
- ↑ Biochemical and genetic analysis of methylenetetrahydrofolate reductase in Leishmania metabolism and virulence. J. Biol. Chem., 2006, s. 38150–8. DOI: 10.1074/jbc.M608387200. PMID 17032644.
- ↑ Oxygen Is the High-Energy Molecule Powering Complex Multicellular Life: Fundamental Corrections to Traditional Bioenergetics. ACS Omega, 2020, s. 2221–2233. DOI: 10.1021/acsomega.9b03352. PMID 32064383.
- ↑ Stryer, Lubert; Berg, Jeremy Mark; Tymoczko, John L.. Biochemistry. San Francisco : W. H. Freeman, 2007. Dostupné online. ISBN 0-7167-8724-5. Archivované 2007-05-18 na Wayback Machine
- ↑ Stoichiometry and compartmentation of NADH metabolism in Saccharomyces cerevisiae. FEMS Microbiol. Rev., 2001, s. 15–37. DOI: 10.1111/j.1574-6976.2001.tb00570.x. PMID 11152939.
- ↑ Rich PR. The molecular machinery of Keilin's respiratory chain. Biochem. Soc. Trans., 2003, s. 1095–105. Dostupné online. DOI: 10.1042/BST0311095. PMID 14641005. Archivované 2019-02-23 na Wayback Machine
- ↑ Redox Transfer across the Inner Chloroplast Envelope Membrane. Plant Physiol, 1991, s. 1131–1137. DOI: 10.1104/pp.95.4.1131. PMID 16668101.
- ↑ a b Nicholls DG; Ferguson SJ. Bioenergetics 3. 1st. vyd. [s.l.] : Academic Press, 2002. ISBN 978-0-12-518121-1.
- ↑ The interaction between the cytosolic pyridine nucleotide redox potential and gluconeogenesis from lactate/pyruvate in isolated rat hepatocytes. Implications for investigations of hormone action. J. Biol. Chem., 15 October 1985, s. 12748–53. Dostupné online. DOI: 10.1016/S0021-9258(17)38940-8. PMID 4044607. Archivované 2008-04-12 na Wayback Machine
- ↑ Energy conservation in Nitrobacter. FEMS Microbiology Letters, 1990, s. 157–62. DOI: 10.1111/j.1574-6968.1990.tb03989.x.
- ↑ Genome Sequence of the Chemolithoautotrophic Nitrite-Oxidizing Bacterium Nitrobacter winogradskyi Nb-255. Appl. Environ. Microbiol., 2006, s. 2050–63. DOI: 10.1128/AEM.72.3.2050-2063.2006. PMID 16517654.
- ↑ Ziegler M. New functions of a long-known molecule. Emerging roles of NAD in cellular signaling. Eur. J. Biochem., 2000, s. 1550–64. DOI: 10.1046/j.1432-1327.2000.01187.x. PMID 10712584.
- ↑ a b Introduction to poly(ADP-ribose) metabolism. Cell. Mol. Life Sci., 2005, s. 721–30. DOI: 10.1007/s00018-004-4503-3. PMID 15868397.
- ↑ The new life of a centenarian: signaling functions of NAD(P). Trends Biochem. Sci., 2004, s. 111–8. DOI: 10.1016/j.tibs.2004.01.007. PMID 15003268.
- ↑ New Embo Member's Review: Functional aspects of protein mono-ADP-ribosylation. EMBO J., 2003, s. 1953–8. DOI: 10.1093/emboj/cdg209. PMID 12727863.
- ↑ a b Bürkle A. Poly(ADP-ribose). The most elaborate metabolite of NAD+. FEBS J., 2005, s. 4576–89. DOI: 10.1111/j.1742-4658.2005.04864.x. PMID 16156780.
- ↑ Ecto-ADP-ribosyltransferases (ARTs): emerging actors in cell communication and signaling. Curr. Med. Chem., 2004, s. 857–72. DOI: 10.2174/0929867043455611. PMID 15078170.
- ↑ LC/MS analysis of cellular RNA reveals NAD-linked RNA. Nat Chem Biol, December 2009, s. 879–881. DOI: 10.1038/nchembio.235. PMID 19820715.
- ↑ Guse AH. Biochemistry, biology, and pharmacology of cyclic adenosine diphosphoribose (cADPR). Curr. Med. Chem., 2004, s. 847–55. DOI: 10.2174/0929867043455602. PMID 15078169.
- ↑ Guse AH. Regulation of calcium signaling by the second messenger cyclic adenosine diphosphoribose (cADPR). Curr. Mol. Med., 2004, s. 239–48. DOI: 10.2174/1566524043360771. PMID 15101682.
- ↑ Guse AH. Second messenger function and the structure-activity relationship of cyclic adenosine diphosphoribose (cADPR). FEBS J., 2005, s. 4590–7. DOI: 10.1111/j.1742-4658.2005.04863.x. PMID 16156781.
- ↑ Sirtuins: Sir2-related NAD-dependent protein deacetylases. Genome Biol, 2004, s. 224. DOI: 10.1186/gb-2004-5-5-224. PMID 15128440.
- ↑ The Sir2 family of protein deacetylases. Annu. Rev. Biochem., 2004, s. 417–35. Dostupné online. DOI: 10.1146/annurev.biochem.73.011303.073651. PMID 15189148. Archivované 2020-12-04 na Wayback Machine
- ↑ The role of NAD+ dependent histone deacetylases (sirtuins) in ageing. Curr Drug Targets, 2006, s. 1553–60. DOI: 10.2174/1389450110607011553. PMID 17100594.
- ↑ Bacterial DNA ligases. Mol. Microbiol., 2001, s. 1241–8. DOI: 10.1046/j.1365-2958.2001.02479.x. PMID 11442824.
- ↑ A newly identified DNA ligase of Saccharomyces cerevisiae involved in RAD52-independent repair of DNA double-strand breaks. Genes & Development, 1997, s. 1912–24. DOI: 10.1101/gad.11.15.1912. PMID 9271115.
- ↑ a b c A conserved NAD binding pocket that regulates protein-protein interactions during aging. Science, 23 March 2017, s. 1312–1317. DOI: 10.1126/science.aad8242. PMID 28336669.
- ↑ NAD+ surfaces again. Biochem. J., 2004, s. e5–6. DOI: 10.1042/BJ20041217. PMID 15352307.
- ↑ Compartmentation of NAD+-dependent signalling. FEBS Lett., 2011, s. 1651–6. DOI: 10.1016/j.febslet.2011.03.045. PMID 21443875.
- ↑ beta-NAD is a novel nucleotide released on stimulation of nerve terminals in human urinary bladder detrusor muscle. Am. J. Physiol. Renal Physiol., 2006, s. F486–95. Dostupné online. DOI: 10.1152/ajprenal.00314.2005. PMID 16189287. Archivované 2019-02-22 na Wayback Machine
- ↑ a b Beta-nicotinamide adenine dinucleotide is an inhibitory neurotransmitter in visceral smooth muscle. Proc. Natl. Acad. Sci. U.S.A., 2007, s. 16359–64. DOI: 10.1073/pnas.0705510104. PMID 17913880.
- ↑ a b β-nicotinamide adenine dinucleotide is an enteric inhibitory neurotransmitter in human and nonhuman primate colons. Gastroenterology, 2011, s. 608–617.e6. DOI: 10.1053/j.gastro.2010.09.039. PMID 20875415.
- ↑ Storage and secretion of beta-NAD, ATP and dopamine in NGF-differentiated rat pheochromocytoma PC12 cells. Eur. J. Neurosci., 2009, s. 756–68. DOI: 10.1111/j.1460-9568.2009.06869.x. PMID 19712094.
- ↑ Release, neuronal effects and removal of extracellular β-nicotinamide adenine dinucleotide (β-NAD+) in the rat brain. Eur. J. Neurosci., 2012, s. 423–35. DOI: 10.1111/j.1460-9568.2011.07957.x. PMID 22276961.
- ↑ A lectin receptor kinase as a potential sensor for extracellular nicotinamide adenine dinucleotide in Arabidopsis thaliana. eLife, 2017, s. e25474. DOI: 10.7554/eLife.25474. PMID 28722654.
- ↑ Sauve AA. NAD+ and vitamin B3: from metabolism to therapies. The Journal of Pharmacology and Experimental Therapeutics, March 2008, s. 883–93. DOI: 10.1124/jpet.107.120758. PMID 18165311.
- ↑ Nicotinamide adenine dinucleotide metabolism as an attractive target for drug discovery. Expert Opin. Ther. Targets, 2007, s. 695–705. DOI: 10.1517/14728222.11.5.695. PMID 17465726.
- ↑ NAD Metabolism in Cancer Therapeutics. Frontiers in Microbiology, 2018, s. 622. DOI: 10.3389/fonc.2018.00622. PMID 30631755.
- ↑ NAD- and NADPH-Contributing Enzymes as Therapeutic Targets in Cancer: An Overview. Biomolecules, 2020, s. 358. DOI: 10.3390/biom10030358. PMID 32111066.
- ↑ Swerdlow RH. Is NADH effective in the treatment of Parkinson's disease?. Drugs Aging, 1998, s. 263–8. DOI: 10.2165/00002512-199813040-00002. PMID 9805207.
- ↑ Mechanisms of action of isoniazid. Mol. Microbiol., 2006, s. 1220–7. DOI: 10.1111/j.1365-2958.2006.05467.x. PMID 17074073.
- ↑ The isoniazid-NAD adduct is a slow, tight-binding inhibitor of InhA, the Mycobacterium tuberculosis enoyl reductase: Adduct affinity and drug resistance. Proc. Natl. Acad. Sci. U.S.A., 2003, s. 13881–6. DOI: 10.1073/pnas.2235848100. PMID 14623976.
- ↑ Mycobacterium tuberculosis dihydrofolate reductase is a target for isoniazid. Nat. Struct. Mol. Biol., 2006, s. 408–13. DOI: 10.1038/nsmb1089. PMID 16648861.
- ↑ a b Cofactor mimics as selective inhibitors of NAD-dependent inosine monophosphate dehydrogenase (IMPDH)—the major therapeutic target. Curr. Med. Chem., 2004, s. 887–900. DOI: 10.2174/0929867043455648. PMID 15083807.
- ↑ Nucleoside and non-nucleoside IMP dehydrogenase inhibitors as antitumor and antiviral agents. Curr. Med. Chem., 1999, s. 599–614. PMID 10390603.
- ↑ SIRT1: roles in aging and cancer. BMB Rep, 2008, s. 751–6. DOI: 10.5483/BMBRep.2008.41.11.751. PMID 19017485.
- ↑ Resveratrol prolongs lifespan and retards the onset of age-related markers in a short-lived vertebrate. Curr. Biol., 2006, s. 296–300. DOI: 10.1016/j.cub.2005.12.038. PMID 16461283.
- ↑ Small molecule activators of sirtuins extend Saccharomyces cerevisiae lifespan. Nature, 2003, s. 191–6. DOI: 10.1038/nature01960. PMID 12939617.
- ↑ Sirtuin activators mimic caloric restriction and delay ageing in metazoans. Nature, 2004, s. 686–9. DOI: 10.1038/nature02789. PMID 15254550.
- ↑ Declining NAD+ Induces a Pseudohypoxic State Disrupting Nuclear-Mitochondrial Communication during Aging. Cell, 19 December 2013, s. 1624–1638. DOI: 10.1016/j.cell.2013.11.037. PMID 24360282.
- ↑ Structural biology of enzymes involved in NAD and molybdenum cofactor biosynthesis. Curr. Opin. Struct. Biol., 2002, s. 709–20. DOI: 10.1016/S0959-440X(02)00385-8. PMID 12504674.
- ↑ Cofactor Biosynthesis. [s.l.] : [s.n.], 2001. ISBN 978-0-12-709861-6. DOI:10.1016/S0083-6729(01)61003-3 The biosynthesis of nicotinamide adenine dinucleotides in bacteria, s. 103–19.
- ↑ Meningitis |Lab Manual |Id and Characterization of Hib |CDC
- ↑ The alcoholic ferment of yeast-juice Part II.--The coferment of yeast-juice. Proceedings of the Royal Society of London, 24 October 1906, s. 369–375. DOI: 10.1098/rspb.1906.0070.
- ↑ Fermentation of sugars and fermentative enzymes [online]. Nobel Foundation. Dostupné online. Archivované 2007-09-27 z originálu.
- ↑ Pyridin, der wasserstoffübertragende bestandteil von gärungsfermenten (pyridin-nucleotide). Biochemische Zeitschrift, 1936, s. 291. DOI: 10.1002/hlca.193601901199. (po nemecky)
- ↑ The isolation and identification of the anti-black tongue factor. J. Biol. Chem., 1938, s. 137–49. Dostupné online. DOI: 10.1016/S0021-9258(18)74164-1. Archivované 2009-03-26 na Wayback Machine
- ↑ The effect of a nicotinic acid deficiency upon the coenzyme I content of animal tissues. J. Biol. Chem., 1939, s. 85–93. Dostupné online. DOI: 10.1016/S0021-9258(18)73482-0. Archivované 2009-03-26 na Wayback Machine
- ↑ Kornberg A. The participation of inorganic pyrophosphate in the reversible enzymatic synthesis of diphosphopyridine nucleotide. J. Biol. Chem., 1948, s. 1475–76. Dostupné online. DOI: 10.1016/S0021-9258(18)57167-2. PMID 18098602. Archivované 2009-03-26 na Wayback Machine
- ↑ Esterification of inorganic phosphate coupled to electron transport between dihydrodiphosphopyridine nucleotide and oxygen. J. Biol. Chem., 1 April 1949, s. 611–23. Dostupné online. DOI: 10.1016/S0021-9258(18)56879-4. PMID 18116985.
- ↑ Biosynthesis of diphosphopyridine nucleotide. I. Identification of intermediates. J. Biol. Chem., 1958, s. 488–92. Dostupné online. DOI: 10.1016/S0021-9258(18)64789-1. PMID 13563526. Archivované 2007-12-14 na Wayback Machine
- ↑ Biosynthesis of diphosphopyridine nucleotide. II. Enzymatic aspects. J. Biol. Chem., 1958, s. 493–500. DOI: 10.1016/S0021-9258(18)64790-8. PMID 13563527.
- ↑ Bieganowski, P; Brenner, C. Discoveries of Nicotinamide Riboside as a Nutrient and Conserved NRK Genes Establish a Preiss-Handler Independent Route to NAD+ in Fungi and Humans. Cell, 2004, s. 495–502. DOI: 10.1016/S0092-8674(04)00416-7. PMID 15137942.
- ↑ Nicotinamide mononucleotide activation of new DNA-dependent polyadenylic acid synthesizing nuclear enzyme. Biochem. Biophys. Res. Commun., 1963, s. 39–43. DOI: 10.1016/0006-291X(63)90024-X. PMID 14019961.
- ↑ Pyridine nucleotide metabolites stimulate calcium release from sea urchin egg microsomes desensitized to inositol trisphosphate. J. Biol. Chem., 15 July 1987, s. 9561–8. Dostupné online. DOI: 10.1016/S0021-9258(18)47970-7. PMID 3496336. Archivované 2007-12-14 na Wayback Machine
- ↑ Transcriptional silencing and longevity protein Sir2 is an NAD-dependent histone deacetylase. Nature, 2000, s. 795–800. DOI: 10.1038/35001622. PMID 10693811.
- ↑ Imai S. The NAD World: a new systemic regulatory network for metabolism and aging--Sirt1, systemic NAD biosynthesis, and their importance. Cell Biochemistry and Biophysics, 2009, s. 65–74. DOI: 10.1007/s12013-008-9041-4. PMID 19130305.
- ↑ Imai S. The NAD World 2.0: the importance of the inter-tissue communication mediated by NAMPT/NAD +/SIRT1 in mammalian aging and longevity control. npj Systems Biology and Applications, 2016, s. 16018. DOI: 10.1038/npjsba.2016.18. PMID 28725474.
Pozri aj
upraviťZdroj
upraviťTento článok je čiastočný alebo úplný preklad článku Nicotinamide adenine dinucleotide na anglickej Wikipédii.